
疾病・不具合報告
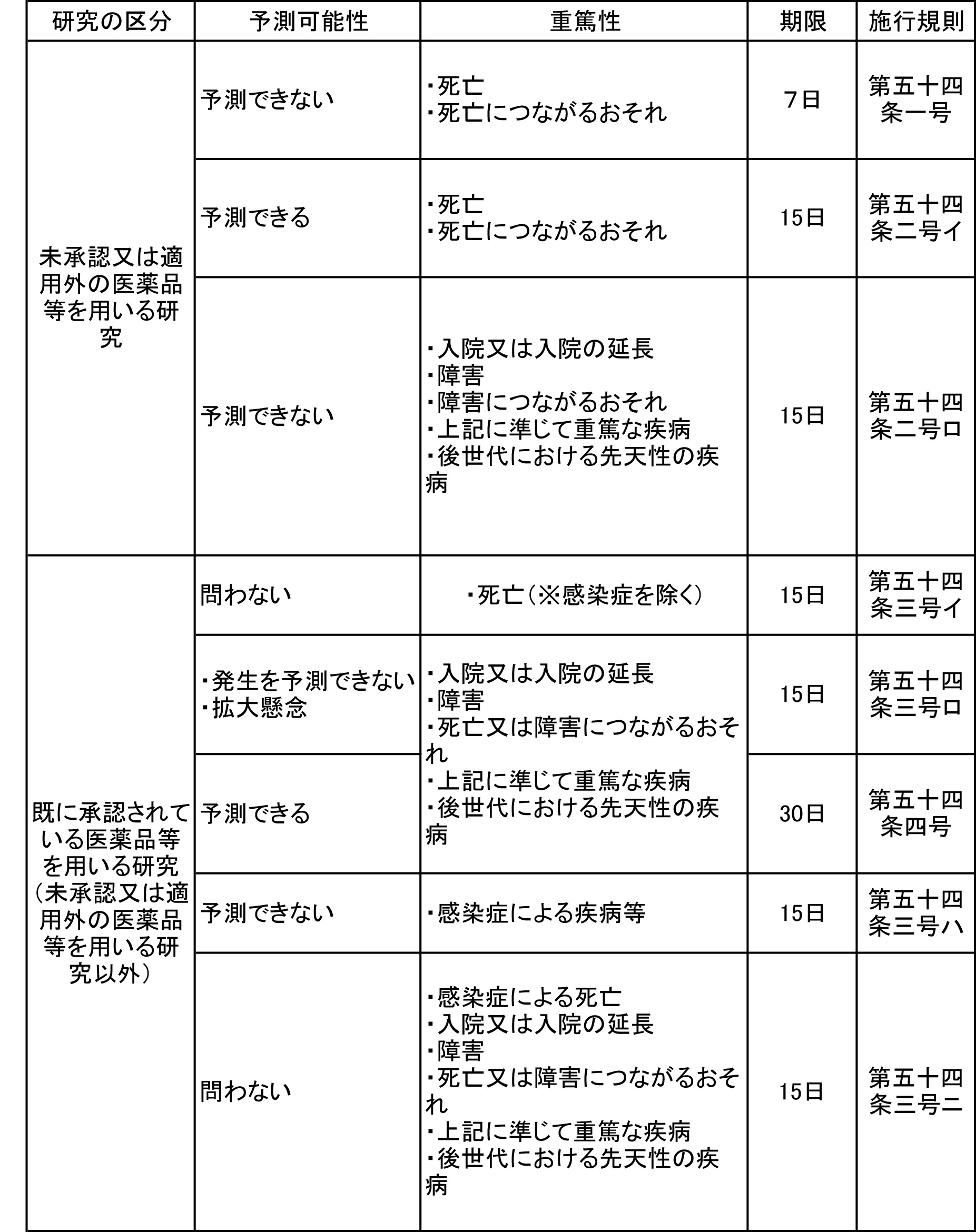
特定臨床研究の実施中に、下記の表に示す疾病・不具合が発生した際には実施医療機関の管理者および認定臨床研究審査委員会に報告することが、研究責任医師に義務付けられています。報告の対象となるのは、特定臨床研究の実施によると疑われる疾病・不具合です。
7日、15日を期限とする報告が遅れた場合、理由書の記載等が求められる可能性があります。
厚生労働大臣への報告については、こちらをご確認ください。
医薬品の特定臨床研究
医療機器・再生医療等製品の特定臨床研究

多施設共同における疾病等報告のフロー
例:A施設で疾病等が発生した場合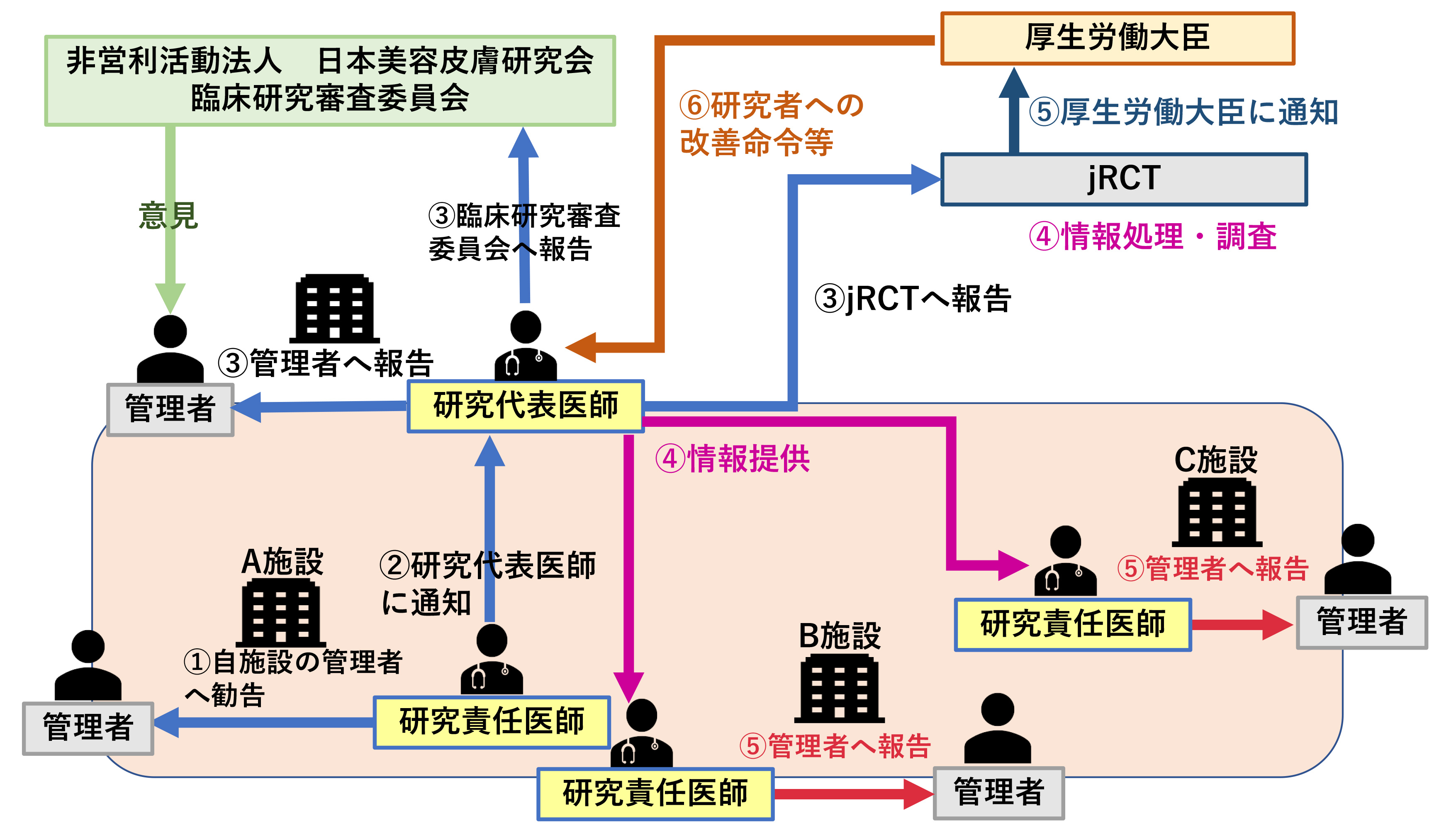
定期報告について
特定臨床研究の実施に起因すると疑われる疾病等のうち、上記の表に該当しない疾病等については、認定臨床研究審査委員会への定期報告時に報告することが定められています。
研究責任医師は、臨床研究の実施状況ならびに疾病等の発生状況について、実施計画を厚生労働大臣に提出した日から1年毎に報告しなければならないと定められています。①実施医療機関の管理者に報告したうえで、②認定臨床研究審査委員会へ報告し、さらに認定臨床研究審査委員会が意見を述べた日から起算して1ヵ月以内に③厚生労働大臣への報告を行なうことが義務付けられています。
①実施医療機関の管理者
②認定臨床研究審査委員会への報告
報告事項
- 臨床研究に参加した対象者の数
- 臨床研究に係る疾病等の発生状況及びその後の経過
- 省令又は研究計画書に対する不適合の発生状況及びその後の対応
- 安全性及び科学的妥当性についての評価
- 管理が必要な利益相反の関与に関する事項
報告時期
実施計画を厚生労働大臣に提出した日から起算して1年ごとに、当該期間満了後2ヵ月以内
提出資料
③厚生労働大臣への報告
報告事項
- 実施計画に記載されている認定臨床研究審査委員会の名称
- 当該委員会による研究継続の適否
- 臨床研究に参加した対象者の数
報告時期
認定臨床研究審査委員会が意見を述べた日から起算して1ヵ月以内
提出資料
- 定期報告書(別紙様式3)

